Tradutor: Paulo Nadanovsky, Rachel Riera
.
Sara Graziadio1, Timothy Hicks1, A. Joy Allen2, Jana Suklan2, Samuel G. Urwin1,
Amanda Winter1, D. Ashley Price1, Richard Body3
1NIHR Cooperação de Diagnósticos In Vitro de Newcastle
Newcastle upon Tyne NHS Hospitals Foundation Trust
Newcastle upon Tyne, NE1 4LP
2NIHR Cooperação de Diagnósticos In Vitro de Newcastle
Universidade de Newcastle, Newcastle upon Tyne, NE2 4HH
3Divisão de Ciências Cardiovasculares, Universidade de Manchester
Universidade de Manchester, Manchester, M13 9PL
Correspondência para sara.graziadio@newcastle.ac.uk
PARECER
O objetivo é desenvolver um padrão de referência composto para o diagnóstico da Covid-19 que apoiará uma abordagem padronizada entre grupos de pesquisa para diminuir a alta taxa de falsos negativos do rRT-PCR que pode prejudicar a avaliação da acurácia diagnóstica de novos testes se o rRT-PCR for usado como o teste de referência sozinho. Atualmente há uma escassez de evidências robustas para o uso de biomarcadores sanguíneos no diagnóstico da Covid-19, portanto, propõe-se que uma extensa lista de biomarcadores seja registrada durante as avaliações de acurácia diagnóstica dos novos testes Covid-19 nos meses de verão, a fim de ajudar a preencher esta lacuna de conhecimento. Para analisar estes dados, será utilizado um Padrão de Referência Composto (PRC) temporário que inclui achados radiológicos para apoiar a identificação de biomarcadores discriminatórios para a Covid-19. Estes serão incluídos na próxima iteração do PRC que poderá ser usado nos estudos de inverno para discriminar a Covid-19 de outras doenças respiratórias altamente prevalentes nos meses de inverno e caracterizadas por aspectos radiológicos semelhantes à Covid-19.
ANTECEDENTES
Os estudos clínicos estão em planejamento ou em andamento e visam avaliar a acurácia diagnóstica no contexto de novos testes diagnósticos. Estes novos testes têm o potencial de serem ferramentas diagnósticas úteis durante as próximas fases da pandemia e para o diagnóstico diferencial durante a fase endêmica. A reação em cadeia da polimerase via transcriptase reversa em tempo real (rRT-PCR) é atualmente o padrão de referência para o diagnóstico da Covid-19, mas uma alta taxa de falsos negativos foi relatada. [1-3] Muitos desses estudos de acurácia diagnóstica comparam os novos testes com a rRT-PCR, um padrão de referência imperfeito. O efeito disto é a subestimação da especificidade dos novos testes.
Os autores propõem o desenvolvimento e uso de um padrão de referência composto, com critérios diagnósticos pré-definidos ou níveis de incerteza diagnóstica, para permitir uma comparação com evidências atualizadas da literatura no que diz respeito à acurácia diagnóstica, mas também com a prática clínica atual no manejo da doença. Múltiplos padrões de referência compostos podem ser desenvolvidos/adaptados para ambientes clínicos específicos, de modo a levar em conta a viabilidade de uso na prática (por exemplo, avaliações em ambientes comunitários não podem contar com exames radiológicos). Entretanto, o foco neste artigo foi o desenvolvimento de um padrão composto de referência para ser usado em estudos hospitalares.
Métodos
Foram realizadas revisões rápidas para identificar sinais e sintomas, biomarcadores e aspectos radiológicos que pudessem apoiar o diagnóstico da Covid-19 (Apêndice I). Estas revisões seguiram uma abordagem de Revisão da Literatura Tradicional (TLR) [4] e apoiaram a discussão de um painel de especialistas que se reuniu no dia 29 de abril de 2020 para identificar os elementos do PRC para o diagnóstico da Covid-19.
O painel foi composto por:
Metodólogos que fazem parte do Instituo Nacional de Pesquisa em Saúde (NIHR) MedTech & Cooperação de Diagnósticos In Vitro (MIC), com experiência em (de):
- Análise e Modelagem de Manuseio Clínico para Diagnóstico In Vitro (MIC Newcastle, MIC London, MIC Leeds)
- Fatores Humanos e Segurança no Design para Diagnóstico In Vitro (MIC London)
- Estatísticas Médicas (MIC Community Healthcaree MIC Newcastle)
Clínicos com experiência em (de):
- Cuidado Ambulatorial, Hospital em Casa (University Hospitals Birmingham NHS Foundation Trust e Oxford Health NHS Foundation Trust)
- Emergência Médica (Manchester University NHS Foundation Trust)
- Doenças Infecciosas (The Newcastle upon Tyne Hospitals NHS Foundation Trust)
- Atenção Primária (Oxford Health NHS Foundation Trust)
Para o desenvolvimento do padrão de referência composto, o viés foi minimizado alinhando nossa metodologia com as seguintes recomendações:[5]
- a utilização da lógica do operador `OR` para ligar testes com sensibilidade perfeita, e a utilização do operador `AND` para ligar testes com especificidade perfeita;
- minimização do número de testes necessários;
- maximização da independência entre os testes componentes (escolhendo testes que medem aspectos biologicamente diferentes da doença);
- potencialmente atribuindo pesos aos testes de forma a incorporar as informações sobre seus diferentes valores clínicos e acurácia no padrão de referência.
Apresentação da evidência
Evidências de estudos avaliando os diferentes componentes potenciais do padrão de referência foram apresentadas como as principais categorias biológicas da testagem. Os dados foram extraídos do BMJ-Best practice para o diagnóstico Covid-19 e identificados através de revisões rápidas da literatura de estudos primários e secundários sobre acurácia diagnóstica [6]:
Sinais e Sintomas (Tabelas 1 e 2)
Biomarcadores Sanguíneos (Tabela 3)
Exames Radiológicos (Tabela 4)
Sinais e Sintomas
Tabela 1. Resumo das evidências dos sinais e sintomas característicos da COVID-19
| Sinais e Sintomas | População de pacientes | Resultados/Limiar | Referência |
| Alteração de olfato/paladar | Leves a moderados | Disfunção olfativa: presente em 86%
Disfunção gustativa: presente em 88% |
Lechien et al 2020
Rhinology; [7] |
| Anorexia | Pacientes hospitalizados | Relatada em 40% dos pacientes | Wang et al 2020 JAMA; [8] |
| Tosse | DE/UTI
Pacientes hospitalizados
Covid-19 confirmada |
Presente em 76%
Presente em 70%
Presente em 58% [IC 95%:41-74%] |
Huang et al 2020 Lancet; [9]
Docherty et al 2020 medRxiv; [10]
Rodriguez-Morales 2020 Travel medicine and infective disease; [11] |
| Dispneia | Pacientes hospitalizados | Presente 18-57%;
Tempo mediano de início 5-8 dias
Presente em 46% [IC 95%:11-80%];
Presente em 65%; |
Rodriguez-Morales 2020 Travel medicine and infective disease; [11]
Huang et al 2020 Lancet; [9]
Docherty et al 2020 medRxiv; [10] |
| Sintomas intestinais (ex.: diarreia) | Pacientes hospitalizados | Presente em 29%, com 4% não tendo outros sintomas | Docherty et al 2020 medRxiv; [10] |
| Fadiga | Pacientes hospitalizados | Relatada em 29% – 69% dos pacientes | Huang et al 2020 Lancet; [9]
|
| Febre | DE/UTI | Presente em 89%
[IC 95%:85-93%];
>=37.8%;
Presente em 69%; |
Huang et al 2020 Lancet; [9]
PHE Guidelines; [12]
Docherty et al 2020 medRxiv; [10] |
| Dor de garganta | Pacientes hospitalizados | Relatada em 5% -17% dos pacientes
Geralmente na fase inicial da doença |
Chen et al 2020 Lancet; [13] |
| Produção de escarro/ Expectoração | Pacientes hospitalizados | Relatada em 26% -33% dos pacientes
|
Huang et al 2020 Lancet; [9]
Wang et al 2020 JAMA; [8] |
DE: Departamentoo de Emergência; IC: Intervalo de confiança; Rx: radiografia; UTI: Unidade de terapia itemsiva
Os autores não conseguiram encontrar artigos relatando a acurácia diagnóstica dos sinais e sintomas em populações não hospitalares. Estes seriam benéficos para informar um padrão de referência para a comunidade e ajudar a entender como os sinais e sintomas se desenvolvem durante o curso da doença.
A única fonte identificada é um artigo de Tostmann (2020) que relatou sinais e sintomas da equipe hospitalar para detecção precoce da Covid-19 (ver Tabela 2):[14]
Tabela 2 Resumo dos sinais e sintomas para detecção precoce da Covid-19 em uma população da equipe hospitalar na Holanda (Tabela reimpressa com permissão de Tostmann, 2020) [14].
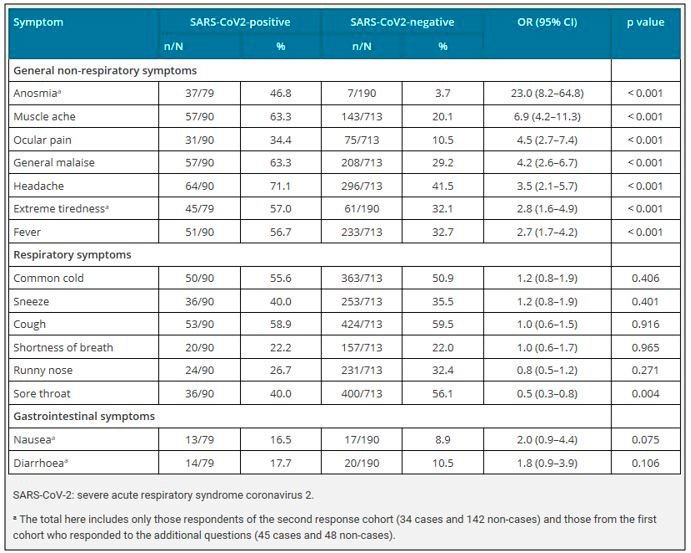
Durante o painel, clínicos relataram que esses sintomas não são específicos da Covid-19 e a única característica a mais da Covid-19 (ou seja, anosmia) poderia, no futuro, estar sujeita a viés devido ao extenso relato e ao potencial de que esse sintoma seja causado por congestão nasal de qualquer etiologia. De fato, como a anosmia foi reconhecida como uma característica da Covid-19 e a informação foi divulgada na mídia em geral, seu valor discriminatório está diminuindo.
Biomarcadores
São raros os artigos que avaliam a acurácia diagnóstica dos biomarcadores sanguíneos. Uma revisão sistemática atualmente sendo realizada pela nossa equipe destacou que a revisão mais abrangente até o momento é de Soraya & Ulhaq, 2020 [15].
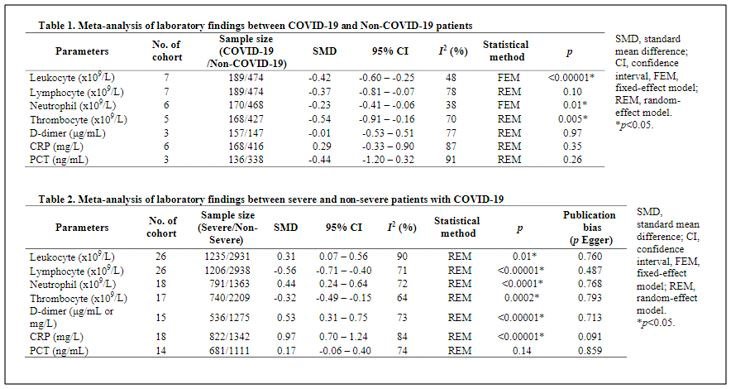
A Tabela 3 apresenta um resumo dos seus resultados laboratoriais:
Tabela 3 Acurácia diagnóstica dos biomarcadores comuns na detecção da COVID-19 (Tabela reimpressa com permissão de Soraya & Ulhaq 2020) [15].
Os clínicos comentaram que leucócitos reduzidos (WBC – white blood cells, em português células sanguíneas brancas), linfócitos e neutrófilos são sinais muito comuns de infecções que não vão ajudar a diferenciar a Covid-19 de outras doenças respiratórias infecciosas durante os meses de inverno, quando estas doenças são prevalentes. O trombócito é um achado menos comum na infecção e tem o potencial de ser útil no diagnóstico diferencial.
Da mesma forma, as características na radiografia e tomografia computadorizada de tórax não são específicas da Covid-19, mas Ai (2020) relata que as taxas positivas de rRT-PCR e tomografia computadorizada de tórax para pacientes diagnosticados com Covid-19 foram de 59% (601/1014) e 88% (888/1014) respectivamente, com uma sensibilidade geral de tomografia computadorizada de tórax de 97% em comparação à PCR[16]:
Tabela 4 Caracterização radiológica para pacientes com suspeita de Covid-19.
| Imagem | Característica | Resultados/Limiar | Referência |
| RX/TC tórax | Pneumonia bilateral | Presente em 72,9% (IC95% 58,6-87,1)
Presente em 100% (n=11) |
Rodriguez-Morales 2020 Travel medicine and infective disease; [11]
Chen N, 2020 (January), Lancet; [13]
Huang et al 2020 Lancet; [9]
|
| Rx/TC tórax | Pneumonia unilateral | Presente em 25% | |
| TC tórax | Opacidade em vidro fosco | Presente em 68,5% (IC95% 51,8 – 85,2 | |
| TC tórax | Consolidação | Presente em 50% (n=1014) | Ai T, 2020 (end of Feb), RSNA Radiology; [16] |
IC: Intervalo de confiança; Rx: radiografia; TC: Tomografia computadorizada
Ai (2020) também mostrou a progressão de opacidade em vidro fosco e consolidação em pacientes ao longo do tempo, indicando que a prevalência de uma característica presente depende do momento em que a radiografia ou TC é tomada durante a progressão da doença.
Discussão
O painel de especialistas decidiu que, embora a proposta de um padrão de referência composto para a Covid-19 fosse interessante para apoiar a padronização de protocolos para estudos de acurácia diagnóstica e fornecer melhores estimativas da acurácia de novos testes, atualmente não há evidências robustas suficientes em torno da acurácia diagnóstica de sinais e sintomas e biomarcadores para que estes possam ser usados como parte de um PRC. Também foi reconhecido que durante o inverno, quando outras doenças respiratórias estiverem circulando, esses sintomas e características serão menos específicos. Portanto, um PRC mais abrangente será necessário para a temporada de inverno, com um PRC mais simples atualmente mais aceitável devido a menor prevalência de outras doenças respiratórias nos meses de verão.
Concluiu-se que a melhor abordagem neste ponto da pandemia é utilizar um PCR temporário, que inclui características radiológicas e rRT-PCR, para apoiar avaliações de novos testes diagnósticos durante o verão, quando há uma baixa prevalência de outras condições respiratórias com assinatura radiológica semelhante à Covid-19. Durante estas avaliações serão coletados dados robustos e padronizados que nos permitirão no início do outono avaliar estatisticamente quais características clínicas são discriminatórias da Covid-19. Uma outra reunião de painel de especialistas será realizada para desenvolver outro PRC, que incorpore os novos resultados sobre características clínicas e biomarcadores a serem utilizados prospectivamente durante as avaliações no inverno, quando outras doenças respiratórias também estiverem circulando, e as evidências radiológicas não serão tão discriminatórias.
Padrão de Referência Composto Temporário para a época de verão
O painel concordou que os seguintes PRCs poderiam ser utilizados até que surjam evidências mais robustas sobre sintomas e biomarcadores:
- COVID-19 CONFIRMADA: qualquer resultado positivo de rRT-PCR durante o curso da doença
- POSSÍVEL COVID-19: PCR/ELISA negativo ou indeterminado E qualquer evidência radiológica de pneumonia com sintomas característicos de COVID-19
- COVID-19 IMPROVÁVEL: PCR/ELISA negativo ou indeterminado E nenhuma evidência radiológica de pneumonia mesmo com sintomas característicos de COVID-19
Deve-se notar que este padrão de referência se refere a uma população de suspeita de Covid-19 com base em uma apresentação sintomática (ou seja, tosse sustentada e/ou febre).
Como uma abordagem de triagem mais ampla no hospital parece ser o próximo estágio da estratégia de testes no Reino Unido, e com o potencial emergente de novos testes para capturar a população não sintomática, é importante incluir pacientes com resultados moleculares positivos, mas sem sintomas característicos da Covid-19, nos estudos de acurácia diagnóstica. É aconselhável recrutar e analisar este grupo de pacientes separadamente com análise exploratória.
Os pacientes não Covid-19 definitivos, ou seja, pacientes sem sintomas e sem positividade do teste rRT-PCR, são excluídos nesta avaliação tardia da acurácia dos novos testes porque é improvável que estratégias futuras de testagem incorporem esta população. Além disso, esta população é normalmente incluída em fases anteriores de avaliação (por exemplo, estudos de validação analítica).
Recomendações para pesquisa
Ao elaborar estudos de acurácia diagnóstica para novos testes diagnósticos de Covid-19, nós aconselhamos os pesquisadores a coletar os dados, sempre que possível, mostrados na Tabela 5 abaixo (além de quaisquer resultados de testes moleculares e sorológicos). Estes dados combinam tanto os indicadores observados na revisão da literatura como os sintomas listados, biomarcadores e indicadores apresentados pelo ISARIC [17].
Tabela 5 Principais características/indicações recomendadas para registro durante a próxima rodada de estudos de acurácia diagnóstica de acordo com o Relato de Caso ISARIC (International Severe Acute Respiratory and Emerging Infections Consortium, em português Consórcio Internacional de Infecções Respiratórias Agudas Graves e Emergentes)[17].
| Sintomas | Biomarcadores | Indicações Adicionais |
| Alteração no olfato/paladar | Troponina cardíaca (cTn-US) | Hipóxia (níveis de saturação) |
| Anorexia
|
PCR – proteína C-reativa | Penumonia unilateral no RX |
| Tosse
|
PCT – Procalcitonina | Pneumonia bilateral no RX |
| Dispneia | LDH – lactato desidrogenase | Opacidade em vidro fosco na TC de tórax |
| Fadiga/cansaço extremo
|
NT-ProBNP – peptídeo natriurético tipo-B | Consolidação na TC de tórax |
| Febre
|
Ferritina sérica | |
| Dor de cabeça
|
Contagem de leucócitos | |
| Dor muscular
|
Contagem de neutrófilos | |
| Dor ocular
|
Contagem de linfóciots | |
| Nariz escorrendo
|
Contagem de eosinófilos | |
| Dor de garganta
|
Dímero-D | |
| Produção de escarro/ Espectoração |
Além dos biomarcadores e sintomas destacados nas revisões de literatura, biomarcadores suplementares e sintomas identificados pelo ISARIC também devem ser capturados onde possível, como mostrado na Tabela 6.
Tabela 6 Características/indicações adicionais recomendadas incluídas no Relato de Caso ISARIC [17].
| Sintomas | Biomarcadores |
| Dor abdominal
|
ALT (alanina aminotransferase) (U/L) |
| Alteração de consciência/confusão
|
RTPa (Razão de Tromboplastina Parcial ativada) |
| Sangramento
|
TTPa (Tempo de Tromboplastina Parcial ativada) |
| Dor no peito
|
AST (Aspartato Aminotransferase) (U/L) |
| Conjuntivite
|
Creatina quinase |
| Diarreia | Creatina
|
| Incapacidade de andar
|
Glicose (mmol/L) |
| Dor articular
|
Hematócrito |
| Retração da parede torácica inferior
|
Hemoglobina |
| Linfadenopatia
|
IL-6 (Interleucina – 6) |
| Náusea/vômito | INR (Razão Normalizada Internacional)
|
| Convulsões | Lactato (mmol/L)
|
| Erupção cutânea
|
Plaquetas |
| Sibilo
|
Potássio |
| TP (Tempo de Protrombina)
|
|
| Sódio
|
|
| Bilirrubina total
|
|
| Ureia (BUN) (mmol/L)
|
|
| WBC (Contagem de glóbulos brancos)
|
A inclusão destes dados adicionais permitiria o desenho futuro do padrão de referência composto para reunir dados de múltiplos estudos com o objetivo de melhorar sua aplicação clínica. Além disso, o início dos sintomas e o momento em que os testes foram realizados devem ser incluídos para permitir a comparação direta entre os estudos e para obter uma compreensão mais profunda do efeito do desenvolvimento da doença e da mudança na prevalência dessas características indicativas ao longo do tempo.
Além disso, à medida que novos testes sorológicos para IgA e IgM são validados, um método de detecção ELISA tem potencial para ser usado independentemente para confirmar a Covid-19 como parte de uma estratégia de testagem mais ampla em diferentes cenários. Esta técnica pode ser particularmente útil nos estágios posteriores da doença quando a taxa de detecção de rRT-PCR cai [18,19]. O uso do anticorpo IgG como parte do padrão de referência precisa ser cuidadosamente considerado, especialmente se estudos futuros confirmarem a presença de anticorpos IgG durante semanas ou meses após a resolução dos sintomas [20].
Entretanto, até que tais testes sejam validados de forma independente para uso clínico, o PRC atual se concentrará apenas nos métodos de testagem existentes, com o objetivo de incorporar ensaios sorológicos para a estação do inverno.
CONCLUSÕES
Nós propusemos um roteiro para estudos de acurácia diagnóstica para a classificação de Covid-19, incluindo a definição de um padrão de referência composto para estudos em andamento, indicações para coleta de dados e considerações em torno da possível introdução de testes de anticorpos no padrão de referência. As recomendações foram baseadas em revisão de literatura e em julgamentos de um painel de especialistas em pesquisa diagnóstica em todo o Reino Unido. Estão sendo realizadas revisões sistemáticas da literatura para atualizar o PRC e a orientação clínica, caso surjam novas evidências.

ESTRATÉGIA DE BUSCA
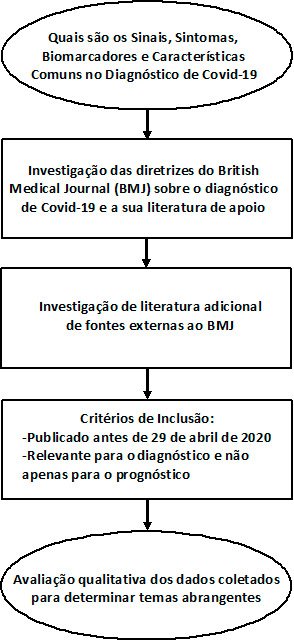
Fim.
Declaração de transparência: o artigo não foi revisado por pares; ele não deve substituir o julgamento clínico individual e as fontes citadas devem ser verificadas. As opiniões expressas neste comentário representam as opiniões dos autores e não necessariamente as da instituição anfitriã, do NHS, do NIHR, ou do Departamento de Saúde e Assistência Social. Os pontos de vista não são um substituto para o aconselhamento médico profissional.
REFERÊNCIAS
- Xiao AT, Tong YX, Zhang S. False-negative of RT-PCR and prolonged nucleic acid onversion in COVID-19: Rather than recurrence. J Med Virol 2020; doi:10.1002/jmv.25855
- Feng H, Liu Y, Lv M, Zhong J. A case report of COVID-19 with false negative RT-PCR test: necessity of chest CT. Jpn J Radiol. 2020;38(5):409‐ doi:10.1007/s11604-020-00967-9
- Green, K., Allen, A., Suklan, J et al.. What Is The Role Of Imaging And Biomarkers Within The Current Testing Strategy For The Diagnosis Of Covid-19? – CEBM [online] CEBM. Available at: <https://www.cebm.net/covid-19/what-is-the-role-of-imaging-and-biomarkers-within-the-current-testing-strategy-for-the-diagnosis-of-covid-19/> [Accessed 13 May 2020].
- Armitage A, Keeble-Ramsay D. The Rapid Structured Literature Review as a Research Strategy. Online Submission, 2009, 6(4), 27-38.
- Naaktgeboren Christiana A, Bertens Loes C M, Smeden Maarten van, Groot Joris A H de, Moons Karel G M, Reitsma Johannes B et al. Value of composite reference standards in diagnostic research BMJ 2013; 347:f5605
- bmj.com. Coronavirus Disease 2019 (COVID-19) – Symptoms, Diagnosis And Treatment | BMJ Best Practice. 2020 [online] Available at: <https://bestpractice.bmj.com/topics/en-gb/3000168> [Accessed 13 May 2020].
- Lechien, J.R., Chiesa-Estomba, C.M., De Siati, D.R. et al. Olfactory and gustatory dysfunctions as a clinical presentation of mild-to-moderate forms of the coronavirus disease (COVID-19): a multicenter European study. Eur Arch Otorhinolaryngol doi:10.1007/s00405-020-05965-1
- Wang D, Hu B, Hu C. Clinical Characteristics of 138 Hospitalized Patients With 2019 Novel Coronavirus–Infected Pneumonia in Wuhan, China. JAMA. 2020;323(11):1061-1069. doi:10.1001/jama.2020.1585
- Huang C, Wang Y, Li X et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. The Lancet, 2020, Volume 395, Issue 10223, 497 – 506 https://doi.org/10.1016/S0140-6736(20)30183-5
- Docherty A B, Harrison E M, Green C A et al. Features of 16,749 hospitalised UK patients with COVID-19 using the ISARIC WHO Clinical Characterisation Protocol. MedRxiv,04.23.20076042. https://doi.org/10.1101/2020.04.23.20076042
- Rodriguez-Morales A, Cardona-Ospina J, Gutiérrez-Ocampo E et al. Clinical, laboratory and imaging features of COVID-19: A systematic review and meta-analysis. Travel Medicine and Infectious Disease 2020: https://doi.org/10.1016/j.tmaid.2020.101623
- PHE Guidelines: https://www.gov.uk/government/collections/coronavirus-covid-19-list-of-guidance [Accessed Date: April 2020]
- Chen N, Zhou M, Dong X et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study The Lancet, 2020 Volume 395, Issue 10223, 507 – 513 https://doi.org/10.1016/S0140-6736(20)30211-7
- Tostmann A, Bradley J, Bousema T et al. Strong associations and moderate predictive value of early symptoms for SARS-CoV-2 test positivity among healthcare workers, the Netherlands. Euro Surveill. 2020;25(16):pii=2000508. https://doi.org/10.2807/1560-7917.ES.2020.25.16.2000508
- Soraya GV, Ulhaq ZS. Crucial Laboratory Parameters in COVID-19 Diagnosis and Prognosis: An Updated Meta-Analysis. SSRN Electronic Journal. 2020 doi:10.2139/ssrn.3576912.
- Ai T, Yang Z, Hou H, Zhan C, et al. Correlation of chest CT and RT-PCR testing in coronavirus disease 2019 (COVID-19) in China: a report of 1014 cases. Radiology. 2020; 200642. 10.1148/radiol.2020200642
- International Severe Acute Respiratory and Emerging Infections Consortium: https://isaric.tghn.org/COVID-19-CRF/ [Accessed May 2020]
- Freeman B, Lester S, Mills L, Ata Ur Rasheed M et al. Validation of a SARS-CoV-2 spike protein ELISA for use in contact investigations and sero-surveillance bioRxiv04.24.057323; doi: https://doi.org/10.1101/2020.04.24.057323
- Liu, W., Liu, L., Kou, G., Zheng, Y., Ding, Y., Ni, W., Wang, Q., Tan, L., Wu, W., Tang, S., Xiong, Z. and Zheng, S. Evaluation of Nucleocapsid and Spike Protein-based ELISAs for detecting antibodies against SARS-CoV-2. Journal of Clinical Microbiology, 2020. DOI: 10.1128/JCM.00461-20
- Long, Q., Liu, B., Deng, H. et al. Antibody responses to SARS-CoV-2 in patients with COVID-19. Nat Med (2020). https://doi.org/10.1038/s41591-020-0897-1
