Tradutores: Paulo Nadanovsky, Ana Luiza Cabrera Martimbianco
Jeffrey K Aronson, Jon Brassey, Kamal R Mahtani
Em nome do Oxford COVID-19 “Evidence Service Team”
Centro de Medicina Baseada em Evidência, Nuffield Department of Primary Care Health Sciences
Universidade de Oxford
Correspondência para jeffrey.aronson@phc.ox.ac.uk
O governo britânico está revendo regularmente as atuais medidas de confinamento, como é exigido por lei a cada 3 semanas. Com o auge da pandemia ainda para chegar ao Reino Unido, parece certo que as medidas atuais vão continuar. Então, quando terminará o confinamento no Reino Unido?
Em 30 de março de 2020, Sir Patrick Vallance, Diretor-Chefe Científico do Governo, deu uma indicação de como esta decisão pode ser orientada, dizendo que o bloqueio britânico estava tendo um “efeito muito grande” sobre o R0, reduzindo-o para “abaixo de um”.
O número ao qual ele se referia é o número básico de reprodução (ou razão reprodutiva) de um vírus, chamado R0 (R nulo ou R zero). E é importante saber como interpretá-lo.
No final, incluímos algumas definições no quadro.
O número básico de reprodução
O número básico de reprodução é definido como o número de casos que se espera que ocorra em média em uma população homogênea como resultado da infecção por um único indivíduo, quando a população é suscetível no início de uma epidemia, antes que a imunidade generalizada comece a se desenvolver e antes que qualquer tentativa de imunização tenha sido feita. Assim, se uma pessoa desenvolve a infecção e a transmite para outras duas, o R0 é 2.
Se a média do R0 na população for maior que 1, a infecção se espalhará exponencialmente. Se o R0 for menor que 1, a infecção se espalhará apenas lentamente, e eventualmente desaparecerá. Quanto maior o valor de R0, mais rapidamente uma epidemia progredirá.
O R0 é estimado a partir de dados coletados no campo e inseridos em modelos matemáticos. O valor estimado depende do modelo utilizado e dos dados que o informam.
O R0 é influenciado por:
- o tamanho da população e a proporção de pessoas suscetíveis no início;
- pela infecciosidade do organismo;
- a taxa de desaparecimento de casos por cura/recuperação ou morte, o primeiro dos quais depende do tempo em que um indivíduo é infectante;
Quanto maior a população, mais pessoas são suscetíveis, e quanto mais infectante o vírus, maior será o R0 para um determinado vírus; quanto mais rápida a taxa de remoção de indivíduos infectados, por cura/recuperação ou morte, menor será o R0.
O zero em “R zero” significa que ele é estimado quando há imunidade zero na população, mesmo que nem todos sejam necessariamente suscetíveis à infecção, embora essa seja a premissa usual. Em uma epidemia com um vírus completamente novo, quanto mais cedo as mensurações forem feitas, mais próximo o valor calculado estará do valor real de R0, assumindo dados de alta qualidade. Por este motivo, é melhor falar sobre a transmissibilidade do vírus no momento em que isto é medido usando um símbolo diferente, Re, o número de reprodução efetivo.
O número de reprodução efetivo, Re
O número de reprodução efetivo, Re, às vezes também chamado de Rt, é o número de pessoas em uma população que pode ser infectado por um indivíduo em qualquer momento específico. Ele muda conforme a população se torna cada vez mais imunizada, seja pela imunidade individual após a infecção ou pela vacinação, e também conforme as pessoas morrem.
O Re é influenciado pelo número de pessoas com a infecção e pelo número de pessoas suscetíveis com as quais as pessoas infectadas estão em contato. O comportamento das pessoas (por exemplo, distanciamento social) também pode afetar o Re.
O número de suscetíveis cai conforme as pessoas morrem ou ficam imunizadas pela exposição. Quanto mais cedo as pessoas se curam/recuperam ou morrem, menor será o valor de Re em um determinado momento.
Infelizmente, o símbolo R0 é frequentemente usado em publicações quando o que se quer dizer é Re. Isto pode ser confuso.
Imunidade de rebanho
Relatos iniciais sugeriram que uma das estratégias do governo britânico para enfrentar a pandemia era permitir que o vírus se espalhasse dentro da comunidade, de forma controlada, para que a imunidade, a chamada imunidade de rebanho, pudesse se desenvolver em toda a população. Entretanto, o secretário de saúde, Matt Hancock, disse mais tarde que isso não fazia parte da resposta do Reino Unido ao vírus. Em contrapartida, outros países, como a Suécia, responderam à pandemia de forma a evitar o confinamento total. O problema de deixar as pessoas pegarem a infecção espontaneamente, levando à imunidade de rebanho, é que a taxa de mortalidade aumentaria. Por exemplo, no dia 10 de abril, o número de casos confirmados na Suécia foi de 9685 com 870 mortes (9,0%), comparado com a Noruega com 6219 casos confirmados e 108 mortes (1,7%) e a Dinamarca com 5830 casos confirmados e 237 mortes (4,4%).
O R0 prevê a extensão da imunização que uma população requer para que a imunidade de rebanho seja alcançada, a propagação da infecção limitada, e a população protegida contra infecções futuras. Para prevenir a disseminação sustentada da infecção, a proporção da população que tem que ser imunizada (Pi) tem que ser maior que 1 – 1/R0. A relação entre Pi e 1 – 1/R0 é mostrada na Figura 1.
Por exemplo, se o R0 = 2, a imunização precisa ser alcançada em 50% da população. Entretanto, se o R0 = 5, a proporção sobe acentuadamente para 80%. Além disso, o aumento é menos acentuado; um aumento de R0 para 10 aumenta a necessidade de imunização para 90%. O sarampo tem um R0 maior que 10, por isso a imunização de uma grande proporção da população é tão importante para a prevenção da doença.
Assim, se o R0 for 10, uma criança com sarampo infectará outras 10 se elas forem suscetíveis. Quando outras crianças ficarem imunes, a criança infectada que encontrar 10 crianças não será capaz de infectar todas elas; o número de infectados dependerá do Re. Quando a imunidade é de 90% ou mais, as chances da criança encontrar crianças não imunizadas o suficiente para transmitir a doença cai para perto de zero, e a população é protegida.
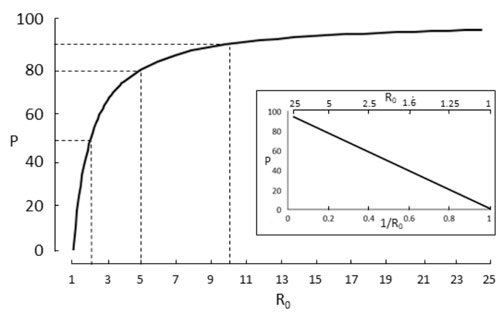
Figura 1. A relação entre o número básico de reprodução de um vírus, R0, e a proporção da população que precisa ser imunizada para atingir a imunidade de rebanho; observe a elevação acentuada da curva nos valores de R0 entre 1 e 5; três exemplos são mostrados: R0 =2, proporção = 50%; R0 = 5, proporção = 80%; R0 = 10, proporção = 90%; o gráfico menor mostra uma linearização do gráfico principal, gerada pela plotagem de P contra 1/R0
A qualquer momento, Re = R0 × (1 – Pi), onde Pi é a proporção da população que está imune naquele momento. Isto é ilustrado na Figura 2.
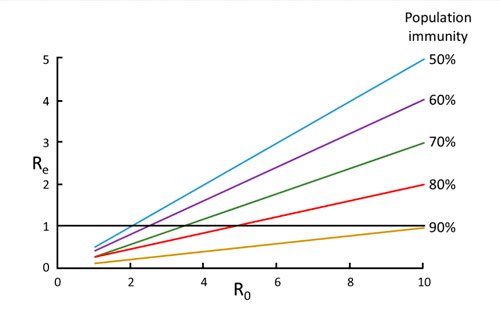
Figura 2. A relação entre R0 e Re em diferentes níveis de imunidade da população
Por exemplo, a imunização de 50% da população (linha azul) trará o Re abaixo de um apenas se o R0 não for maior que 2; em contraste, a imunização de 90% da população (linha marrom) trará o Re abaixo de 1 ou menos para todos os valores de R0 até 10.
Como o R0 é estimado
Um modelo epidemiológico típico pelo qual o R0 é estimado baseia-se em três fatores: a susceptibilidade individual à infecção, a taxa na qual as infecções realmente ocorrem (Infectividade) e a taxa de remoção da infecção da população, seja pela cura/recuperação ou pela morte. Este é o chamado modelo S-I-R. O modelo envolve a solução de equações diferenciais lineares simultâneas e foi descrito em 1927 por W. O. Kermack e A. G. McKendrick. Uma versão desse modelo é mostrada na Figura 3.

Figura 3. Uma versão do modelo descrito por Kermack & McKendrick (Proc Roy Soc A 1927; 115: 700-21); os dados podem ser inseridos no modelo e as diferentes taxas em que os eventos ocorrem e os números de reprodução básica ou efetiva calculados
Entretanto, muitos outros métodos têm sido utilizados, incluindo tanto modelos estatísticos quanto cálculos simples. Os primeiros variam desde métodos como o modelo estocástico Reed-Frost, desenvolvido por Lowell J. Reed e Wade Hampton Frost em 1928, semelhante a um método que já estava sendo desenvolvido por H E Soper e que ele descreveu em 1929, até o método IDEA, descrito pela primeira vez por Fisman e colaboradores em 2013. Dos métodos que envolvem o cálculo matemático simples do R0, um que é comumente utilizado envolve a seguinte equação: R0 = βS/γ, onde β é a taxa de transmissão, S é o número de suscetíveis no início da epidemia, e γ é a taxa de remoção. Existem muitas outras variantes de natureza similar.
A Figura 4 mostra uma comparação dos valores estimados de R0 para uma gama de vírus, resumidos a partir de uma variedade de fontes publicadas. O gráfico mostra como os valores estimados de R0 podem ser variáveis de vírus para vírus. Entretanto, os números devem ser interpretados com cautela pois, uma vez que a qualidade dos dados nos quais foram baseados terá variado de estudo para estudo, os dados terão sido coletados em momentos diferentes durante o curso da propagação do vírus (por exemplo, comparar influenza na primavera e outono de 1918), e os modelos utilizados terão sido diferentes. Também deve ficar claro no gráfico, embora os dados de mortalidade não sejam mostrados, que o R0 não está relacionado com a taxa de letalidade.

Figura 4. Valores estimados de R0 em diferentes infecções virais, obtidas de diversas fontes publicadas
Qual é o R0 do SARS-CoV-2?
As estimativas do R0 do SARS-CoV-2 variam muito. A Figura 5 mostra nove estimativas, todas de estudos na China ou Coreia do Sul. A estimativa média do R0 é 2,63 (IC 95% = 1,85 – 3,41). A estimativa média de um levantamento mais amplo de 16 estimativas publicadas, é de 2,65 (1,97 – 3,09). Em ambos os casos, a variação é de 0,4 a 4,6.

Figura 5. Nove estimativas de R0 em estudos para os quais havia informações sobre o tempo em que as mensurações foram feitas, de 1 de dezembro (dia 1) a 6 de março (dia 97); os dados são de estudos na China continental (vermelho), Wuhan (preto), Shenzhen (azul) e Coréia do Sul (verde); os resultados mostram o grande grau de variabilidade nas estimativas médias, atribuível a variações na qualidade dos dados e nos modelos utilizados; entretanto, cinco dos resultados se agrupam em torno de 2,6.
Isto significa que, para nos proteger contra epidemias futuras, será necessária uma imunidade de rebanho de cerca de 62%, tomando a estimativa média em todos estes estudos. Tomando o valor mais alto (4,6), será necessária uma imunização de 78%, e seria prudente objetivar pelo menos isto. Quando um teste para detectar anticorpos contra o SARS-CoV-2 e uma vacina estiverem disponíveis, seremos capazes de dizer até que ponto a população foi imunizada por exposição e por vacinação.
No Reino Unido, uma das principais descobertas que influenciaram a decisão do governo de iniciar o confinamento foi o modelo apresentado pela equipe do COVID-19 do Imperial College. O modelo explora o efeito de duas estratégias (a) supressão, pela qual são instituídas intervenções para levar o Re abaixo de 1, e (b) mitigação, pela qual são instituídas estratégias para reduzir o impacto da epidemia, mas sem interromper completamente a transmissão viral, reduzindo assim o Re, mas não necessariamente abaixo de 1. O modelo presumiu um R0 de cerca de 2,4 e previu que, na ausência de quaisquer medidas de controle, 81% da população do Reino Unido ficaria infectada, com mais de meio milhão de mortes. Entretanto, este número poderia ser reduzido para menos de 50.000 (e possivelmente menos de 6.000 mortes) com um conjunto de estratégias de supressão em vigor. Não é de se admirar que, diante desses números, o governo do Reino Unido tenha iniciado rapidamente o confinamento.
É importante notar que o valor do R0 varia consideravelmente nos modelos utilizados na pandemia da COVID-19. Uma revisão sistemática relatou que a média de 29 valores relatados de R0 de 21 estudos foi estimada em 3,32 (2,81-3,82), com uma variação de 1,9 a 6,49; todos os estudos incluídos eram da China. Em declaração de 23 de janeiro de 2020 sobre o surto da COVID-19, a Organização Mundial da Saúde (OMS) deu uma estimativa preliminar do R0 de 1,4-2,5.
Interpretando as notícias
Os dados chineses sugerem pouca alteração nos números de reprodução mensurados em vários momentos ao longo dos últimos 3 meses. Portanto, ao ler um relato de que o número de reprodução (Re) caiu abaixo de 1, o que deve ser motivo de alegria, seja cauteloso. O valor calculado depende da qualidade dos dados, que podem ser ruins, e do modelo epidemiológico utilizado, que pode distorcer o resultado. Lembre-se das palavras sábias de George Box sobre os modelos:
“Todos os modelos estão errados, mas alguns modelos são úteis”.
Ou como ele colocou, menos dramaticamente, mas mais especificamente:
“Os modelos, é claro, nunca são verdadeiros, mas felizmente é apenas necessário que sejam úteis”. Para isso, geralmente é preciso apenas que eles não sejam grosseiramente errados”.
Definições
Algumas definições dos termos utilizados neste artigo são fornecidas abaixo.
Imunidade a uma infecção viral é o estado de ser não suscetível a ela, em virtude de poder produzir anticorpos neutralizantes quando atacado por ela; tais anticorpos podem ser produzidos por exposição prévia ou por imunização após a vacinação.
A imunidade de rebanho é uma forma de proteção contra uma doença infecciosa que resulta quando uma grande proporção da população se tornou imune, conferindo proteção indireta contra a infecção a indivíduos que não são imunes.
A vacinação contra uma infecção viral é a administração de uma vacina a um indivíduo com a intenção de imunizar esse indivíduo ou impulsionar a imunidade pré-existente.
A imunização contra uma infecção viral é a produção de imunidade à infecção em virtude de uma vacinação bem sucedida ou exposição ao vírus.
Aviso: o artigo não foi revisado por pares; ele não deve substituir o julgamento clínico individual e as fontes citadas devem ser verificadas. As opiniões expressas neste comentário representam as opiniões dos autores e não necessariamente as da instituição anfitriã, do NHS, do NIHR, ou do Departamento de Saúde e Assistência Social. Os pontos de vista não são um substituto para o aconselhamento médico profissional.
